Saúde
Anvisa suspende de forma cautelar 12 milhões de doses da CoronaVac
Agência Nacional de Vigilância Sanitária alega que vacinas foram envasadas em fábrica não inspecionada por autoridades brasileiras
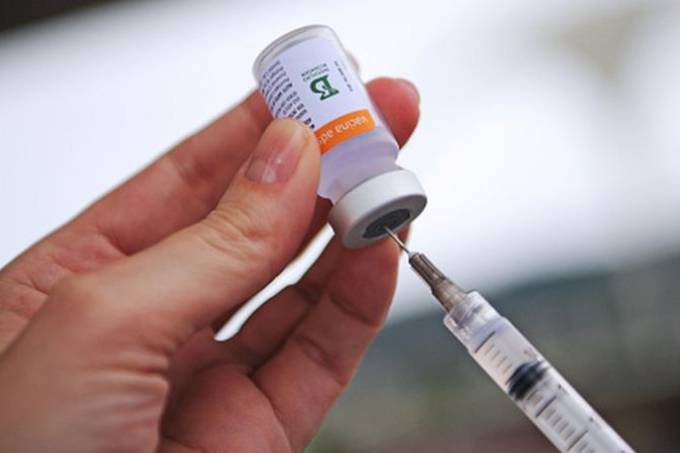
A CoronaVac foi a primeira vacina contra a Covid-19 a começar a ser aplicada no Brasil – Reprodução/Getty Images
A Agência Nacional de Vigilância Sanitária (Anvisa) determinou, neste sábado, 4, a interdição cautelar de mais de 12 milhões de doses da CoronaVac. De acordo com a agência, a medida ocorreu porque os imunizantes foram envasados em uma unidade fabril que não foi inspecionada pelas autoridades sanitárias brasileiras e não está aprovada na Autorização de Uso Emergencial emitida pelo órgão.
Na última sexta-feira, em reunião, o Instituto Butantan, responsável pela fabricação e importação da Coronavac no Brasil, informou à Anvisa que 25 lotes foram enviados para o Brasil pela Sinovac, empresa chinesa que desenvolveu o vacina. O instituto reportou ainda que outras 9 milhões de doses, distribuídas em dezessete lotes e também envasadas no local, estão em tramitação de envio e liberação ao país.
Os lotes envolvidos, segundo a Anvisa, são: 202107101H, 202107102H, 202107103H, 202107104H, 202108108H, 202108109H, 202108110H, 202108111H, 202108112H, 202108113H, 202108114H, 202108115H, 202108116H, L202106038, J202106025, J202106029, J202106030, J202106031, J202106032, J202106033, H202106042, H202106043, H202106044, J202106039, L202106048.
A Anvisa informou que avaliou a documentação apresentada pelo Butantan e consultou as bases de dados internacionais, em busca de informações acerca das condições de boas práticas de fabricação da empresa responsável pelo envase desses lotes. Mas, até o momento, não localizou nenhum relatório de inspeção emitido por outras autoridades de referência reconhecidas internacionalmente. A agência decidiu, assim, agir para mitigar um possível risco sanitário, proibindo o uso dos lotes envasados na planta não
aprovada evedando a distribuição das doses ainda não encaminhados às unidades de saúde.
A Anvisa pretende ainda identificar e monitorar o estado de saúde das pessoas que porventura foram vacinadas com doses dos lotes interditados e trabalhar para regularizar a situação da planta onde os imunizantes foram envasados.
O Butantan enviou a seguinte nota sobre o assunto:
O Butantan esclarece que a medida da Anvisa não deve causar alarmismo. Foi o próprio Instituto que, por compromisso com a transparência e por extrema precaução, comunicou o fato à agência, após atestar a qualidade das doses recebidas. Isso garante que os imunizantes são seguros para a população.
O Instituto Butantan encaminhou à Anvisa há 15 dias toda a documentação necessária para a certificação do processo de produção em que foram feitas essas doses. Por isso, tem convicção que ela será concedida em breve. Caso necessário, pode complementar a solicitação com mais dados, inclusive da Sinovac, caso a agência julgue necessário.
A vacina do Butantan é o imunizante mais seguro à disposição do Programa Nacional de Imunizações (PNI), por causa da sua plataforma de vírus inativado. Todos os lotes liberados pelo instituto estão de posse do Ministério da Saúde, como firmado em contrato. Reafirmamos, no entanto, que todas as doses que saíram da unidade fabril estão atestadas pelo rigoroso controle de qualidade do Butantan.
Informa, ainda, que 6 milhões de doses da vacina do Butantan, que fazem parte de um lote de 12 milhões de imunizantes formuladas no site fabril da zona oeste de SP, aguardavam liberação da Anvisa. Na última quinta-feira (2), o órgão regulatório liberou e as mesmas foram expedidas na sexta-feira (3).
Esse pedido de liberação ao órgão regulatório aconteceu por uma mudança em uma das etapas do processo de formulação da vacina, que pode ocorrer no decorrer da fabricação. A fábrica onde é feita a formulação e o envase da CoronaVac são todas certificadas pela Anvisa, desde o final de 2020.
O Butantan convida a cúpula da Anvisa para voltar a conhecer as instalações das fábricas da Sinovac, na China, e reforça o seu compromisso com a saúde pública, que é comprovado ao longo de seus 120 anos de história.
Fonte: veja.abril.com.br/

-

 Policial4 dias atrás
Policial4 dias atrásUrgente: “Três Homens Encapuzados Cometem Furto em Comércio no Bairro Santa Felicidade em Alta Floresta D´Oeste”
-

 Garota Expoalta1 dia atrás
Garota Expoalta1 dia atrásEnquete de Votação: Vote aqui na Garota Internet 2024
-

 Policial2 dias atrás
Policial2 dias atrásSorveteria é alvo de furto nesta madrugada de terça-feira em Alta Floresta D´Oeste
-

 Nota de Falecimento4 dias atrás
Nota de Falecimento4 dias atrásA Funerária Alta Floresta comunica o falecimento do senhor Augusto Francisco de Sá
-

 Reportagens6 dias atrás
Reportagens6 dias atrásCia de Rodeio 2k Apresenta o 3º Circuito Top Cowboys 2024
-

 Policial6 dias atrás
Policial6 dias atrásAumento de Furtos em Alta Floresta D´Oeste Preocupa Moradores
-

 Nota de Falecimento20 horas atrás
Nota de Falecimento20 horas atrásA Funerária Pax Bom Pastor comunica o falecimento de Ivan Roosevelt Franco Barreto
-

 Policial3 dias atrás
Policial3 dias atrásPolícia Militar recupera motocicleta furtada em Circuito de Rodeio em Alta Floresta

































